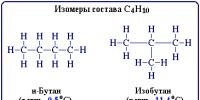
Llojet e gazrave helmues, efektet e tyre në organizëm. Karakteristikat e gazeve shpërthyese dhe të dëmshme Gazi natyror është lloji më i mirë i karburantit
Gazi helmues është një substancë kimike toksike që shkakton dehje të trupit dhe dëmtim të organeve dhe sistemeve të brendshme. Hyn përmes sistemit të frymëmarrjes, lëkurës dhe traktit gastrointestinal.
Lista e gazeve helmuese në varësi të efekteve toksikologjike të tyre:
- Agjentët nervorë - monoksidi i karbonit, sarin.
- Flluska – lewisite, gaz mustardë.
- Asfiksuesit - fosgjen, difosgjen, klor.
- Lehtësuesit e lotëve - bromobenzil cianid, kloroacetofenon.
- Ekspozimi i përgjithshëm: acid hidrocianik, klorur cianogjen.
- Ngacmues – adamsite, CR, CS.
- Psikotomimetik – BZ, LSD-25.
Le të shqyrtojmë gazrat më të rrezikshëm, mekanizmin e shkatërrimit të tyre dhe shenjat e helmimit te njerëzit.
Sarin
 Sarin është helmues substancë e lëngshme, e cila në një temperaturë prej 20 °C avullon shpejt dhe ka një efekt nervor-paralitik në trupin e njeriut.. Si gaz, është i pangjyrë dhe pa erë dhe është më i rrezikshmi nëse thithet.
Sarin është helmues substancë e lëngshme, e cila në një temperaturë prej 20 °C avullon shpejt dhe ka një efekt nervor-paralitik në trupin e njeriut.. Si gaz, është i pangjyrë dhe pa erë dhe është më i rrezikshmi nëse thithet.
Simptomat shfaqen menjëherë pas ekspozimit në traktin respirator. Shenjat e para të helmimit janë vështirësia në frymëmarrje dhe shtrëngimi i bebëzës.
Manifestimet klinike:
- acarim i mukozës së hundës, shkarkim i lëngshëm;
- jargëzim, të vjella;
- shtrëngim në gjoks;
- gulçim, lëkurë kaltërosh;
- spazma e bronkeve dhe rritja e formimit të mukusit në to;
- edemë pulmonare;
- ngërçe dhe dhimbje të forta në bark.
Nëse avulli i sarinit me përqendrim të lartë hyn në trup Dëmtimi i rëndë i trurit ndodh brenda 1-2 minutash. Një person nuk mund të kontrollojë funksionet fiziologjike të trupit - lëvizjet e pavullnetshme të zorrëve dhe urinimin. Shfaqen konvulsione dhe konvulsione. Koma zhvillohet e ndjekur nga arresti kardiak.
Gaz mustardë
 Gazi mustardë është gaz mustardë. Ky është një përbërës kimik me veprim flluskë. Në formë të lëngshme, substanca ka një erë mustarde. Ai hyn në trup në dy mënyra - nga pikat ajrore dhe nga kontakti i lëngut me lëkurën. Ka tendencë të grumbullohet. Shenjat e helmimit shfaqen pas 2-8 orësh.
Gazi mustardë është gaz mustardë. Ky është një përbërës kimik me veprim flluskë. Në formë të lëngshme, substanca ka një erë mustarde. Ai hyn në trup në dy mënyra - nga pikat ajrore dhe nga kontakti i lëngut me lëkurën. Ka tendencë të grumbullohet. Shenjat e helmimit shfaqen pas 2-8 orësh.
Simptomat e dehjes së gazit nga inhalimi:
- dëmtimi i mukozës së syve;
- lacrimation, fotofobi, ndjenja e rërës në sy;
- thatësi dhe djegie në hundë, pastaj ënjtje të nazofaringit me rrjedhje purulente;
- laringit, trakeit;
- bronkit.
Nëse lëngu hyn në sy, do të shkaktojë verbëri. Në rastet e rënda të helmimit me gaz mustardë, zhvillohet pneumonia dhe vdekja ndodh në ditën e 3-4 nga mbytja.
Simptomat e helmimit me gaz gjatë kontaktit me lëkurën janë skuqja e ndjekur nga formimi i flluskave që përmbajnë lëng seroz, lezione të lëkurës, ulçera, nekrozë. Gazi shkatërron membranat qelizore, prish metabolizmin e karbohidrateve dhe shkatërron pjesërisht ADN-në dhe ARN-në.
Lewisite
 Lewisite është një substancë shumë toksike, avujt e së cilës mund të depërtojnë në veshjet mbrojtëse kimike dhe maskat e gazit. Është një lëng kafe me erë të fortë. Gazi klasifikohet si një vezikant i lëkurës. Vepron në trup menjëherë dhe nuk ka periudhë latente.
Lewisite është një substancë shumë toksike, avujt e së cilës mund të depërtojnë në veshjet mbrojtëse kimike dhe maskat e gazit. Është një lëng kafe me erë të fortë. Gazi klasifikohet si një vezikant i lëkurës. Vepron në trup menjëherë dhe nuk ka periudhë latente.
Simptomat e helmimit me gaz kur lëkura preket zhvillohen brenda 5 minutave:
- dhimbje dhe djegie në pikën e kontaktit;
- ndryshime inflamatore;
- skuqje e dhimbshme;
- formimi i flluskave, ato hapen shpejt;
- shfaqja e erozioneve, të cilat duhen disa javë për t'u shëruar;
- në raste të rënda, kur ekspozohen ndaj përqendrimeve të mëdha të lewisitit, formohen ulçera të thella.
Simptomat gjatë thithjes së gazit:
- dëmtimi i mukozës së nazofaringit, trakesë, bronkeve;
- lëngu nga hunda;
- teshtitje, kollitje;
- dhimbje koke;
- nauze, të vjella;
- humbja e zërit;
- ndjenja e presionit në gjoks, gulçim.
Mukoza e syve është shumë e ndjeshme ndaj gazit helmues.. Bëhet e kuqe, qepallat fryhen dhe lakrimi rritet. Një person përjeton një ndjesi djegieje në sy. Kur lewiziti i lëngshëm hyn në traktin gastrointestinal, viktima fillon të derdhet shumë dhe të vjella. Shfaqen dhimbje të forta në zgavrën e barkut. Organet e brendshme janë të prekura dhe presioni i gjakut bie ndjeshëm.
Sulfide hidrogjenit
 Sulfidi i hidrogjenit është një gaz pa ngjyrë me një erë të fortë vezësh të kalbura. Në përqendrime të larta substanca është shumë toksike. Hyrja në trup me frymëmarrje, zhvillohen simptoma të dehjes së përgjithshme - dhimbje koke, marramendje, dobësi. Sulfidi i hidrogjenit absorbohet shpejt në gjak dhe ndikon në sistemin nervor qendror.
Sulfidi i hidrogjenit është një gaz pa ngjyrë me një erë të fortë vezësh të kalbura. Në përqendrime të larta substanca është shumë toksike. Hyrja në trup me frymëmarrje, zhvillohen simptoma të dehjes së përgjithshme - dhimbje koke, marramendje, dobësi. Sulfidi i hidrogjenit absorbohet shpejt në gjak dhe ndikon në sistemin nervor qendror.
Shenjat e helmimit me gaz:
- shije metalike në gojë;
- paraliza e nervit përgjegjës për shqisën e nuhatjes, kështu që viktima menjëherë pushon të ndjejë ndonjë erë;
- dëmtimi i rrugëve të frymëmarrjes, edemë pulmonare;
- ngërçe të rënda;
- koma.
Oksid karboni
Monoksidi i karbonit është një substancë helmuese pa ngjyrë, më e lehtë se ajri. Duke hyrë në trup përmes rrugëve të frymëmarrjes, ai absorbohet shpejt në gjak dhe lidhet me hemoglobinën. Kjo bllokon transportin e oksigjenit në të gjitha qelizat, ndodh uria e oksigjenit dhe frymëmarrja qelizore ndalon. 
Simptomat e helmimit me monoksid karboni:
- marramendje dhe dhimbje koke;
- frymëmarrje e shpejtë dhe rrahje zemre, gulçim;
- zhurma në vesh;
- mprehtësia vizuale e dëmtuar, dridhje në sy;
- skuqje e lëkurës;
- nauze, të vjella.
Në helmime të rënda vërehen konvulsione. Simptomat që i paraprijnë komës rriten - një rënie e presionit të gjakut, dobësi e rëndë, humbje e vetëdijes. Në mungesë të ndihmës mjekësore, vdekja ndodh brenda 1 ore.
Fosgjeni
Fosgjeni është një gaz pa ngjyrë me erën e barit të kalbur. Substanca është e rrezikshme nëse thithet, shenjat e para të dehjes shfaqen pas 4-8 orësh. Në përqendrime të larta, vdekja ndodh brenda 3 sekondave. Gazi që hyn në mushkëri i shkatërron ato, duke shkaktuar ënjtje të menjëhershme.
Simptomat në faza të ndryshme të helmimit: 
- Edema pulmonare fillon të zhvillohet në periudhën latente, kur viktima nuk është në dijeni të helmimit. Sinjalet e para nga trupi janë një shije e ëmbël, e ngurtë në gojë, të përziera. Ndonjëherë ka të vjella. Një person ndjen dhimbje të fytit, kruajtje dhe djegie në nazofaringë. Ndodh një refleks i kollës, frymëmarrja dhe pulsi janë ndërprerë.
- Pas periudhës latente, gjendja e viktimës përkeqësohet ndjeshëm. Shfaqet një kollë e fortë dhe personi fillon të mbytet. Lëkura dhe buzët bëhen blu.
- Faza e përkeqësimit progresiv është presioni i rëndë në gjoks, duke çuar në mbytje, ritmi i frymëmarrjes rritet në 70 në minutë (normale 18). Në mushkëri formohen shumë lëngje dhe mukus për shkak të dekompozimit të alveolave. Një person kollitet me sputum që përmban gjak. Frymëmarrja bëhet e pamundur. 50% e bcc (vëllimit të gjakut qarkullues) shkon në mushkëri dhe i rrit ato. Pesha e një mushkërie mund të jetë 2.5 kg (norma është 500-600 g).
Në raste të rënda, vdekja brenda 10-15 minutave. Në rast të helmimit të moderuar me gaz, vdekja ndodh brenda 2-3 ditëve. Rimëkëmbja mund të ndodhë 2-3 javë pas helmimit, por kjo është e rrallë për shkak të infeksionit.
Acidi hidrocianik
Acidi hidrocianik është një lëng i pangjyrë, i lehtë dhe i lëvizshëm me erë të theksuar. Ai bllokon zinxhirin e lëvizjes së oksigjenit nëpër inde, duke shkaktuar hipoksi të indeve. Gazi ndikon në sistemin nervor, duke prishur inervimin e organeve.
Simptomat e helmimit të frymëmarrjes: 
- dispnea;
- në fillim të zhvillimit të pamjes klinike, frymëmarrje e shpejtë;
- me intoksikim të rëndë - depresion dhe ndërprerje të frymëmarrjes.
Shenjat e zemrës:
- ngadalësimi i rrahjeve të zemrës;
- presioni i rritur i gjakut;
- vazospazma;
- me rritjen e simptomave - rënie të presionit, rritje të rrahjeve të zemrës, dështim akut kardiovaskular, arrest kardiak.
Gazrat helmues janë substanca të forta, me veprim të shpejtë. Për të shpëtuar një person, janë të nevojshme masat emergjente të ringjalljes. Nëse rezultati është i favorshëm, viktima ka nevojë për trajtim afatgjatë rehabilitues.
1. Lëndët e ngurta pezull
Lëndët e ngurta të pezulluara përfshijnë pluhurin, hirin, blozën, tymin, sulfatet dhe nitratet. Në varësi të përbërjes së tyre, ato mund të jenë shumë toksike dhe pothuajse të padëmshme. Substancat e pezulluara formohen si rezultat i djegies së të gjitha llojeve të karburantit: gjatë funksionimit të motorëve të makinave dhe gjatë proceseve të prodhimit. Kur grimcat e pezulluara depërtojnë në sistemin e frymëmarrjes, sistemi i frymëmarrjes dhe i qarkullimit të gjakut prishen. Grimcat e thithura ndikojnë drejtpërdrejt si në traktin respirator ashtu edhe në organet e tjera për shkak të efekteve toksike të përbërësve që përmbahen në grimca. Kombinimi i përqendrimeve të larta të lëndëve të ngurta të pezulluara dhe dioksidit të squfurit është i rrezikshëm. Personat me çrregullime kronike të mushkërive, sëmundje kardiovaskulare, astmë, ftohje të shpeshta, të moshuarit dhe fëmijët janë veçanërisht të ndjeshëm ndaj efekteve të grimcave të vogla të pezulluara. Pluhuri dhe aerosolet jo vetëm që e vështirësojnë frymëmarrjen, por gjithashtu çojnë në ndryshime klimatike, sepse ato reflektojnë rrezatimin diellor dhe e bëjnë të vështirë daljen e nxehtësisë nga Toka. Për shembull, i ashtuquajturi smog në qytetet jugore me popullsi të dendur redukton transparencën e atmosferës me 2-5 herë.
2. Dioksidi i azotit
Një gaz helmues pa ngjyrë, pa erë.
Oksidet e azotit hyjnë në atmosferë nga ndërmarrjet industriale, termocentralet, furrat dhe shtëpitë e kaldajave, si dhe nga automjetet. Ato mund të formohen dhe lëshohen në atmosferë në sasi të mëdha gjatë prodhimit të plehrave minerale. Në atmosferë, emetimet e oksideve të azotit shndërrohen në dioksid azoti. Është një gaz helmues pa ngjyrë, pa erë. Dioksidi i azotit është një komponent i rëndësishëm i proceseve fotokimike në atmosferë që lidhen me formimin e ozonit në mot me diell. Në përqëndrime të ulëta të dioksidit të azotit, vërehen probleme me frymëmarrjen dhe kollitje. Organizata Botërore e Shëndetësisë ka zbuluar se një përqendrim mesatar në orë i dioksidit të azotit prej 400 μg/m3 shkakton simptoma të dhimbshme te pacientët me astmë dhe grupe të tjera njerëzish me mbindjeshmëri. Me një përqendrim mesatar vjetor prej 30 mcg/m3, rritet numri i fëmijëve me frymëmarrje të shpejtë, me kollitje dhe të pacientëve me bronkit. Dioksidi i azotit zvogëlon rezistencën e trupit ndaj sëmundjeve, redukton hemoglobinën në gjak dhe irriton traktin respirator. Me thithjen e zgjatur të këtij gazi, ndodh uria e oksigjenit e indeve, veçanërisht tek fëmijët. Shkakton sëmundje të frymëmarrjes dhe qarkullimit të gjakut dhe neoplazi malinje. Çon në përkeqësimin e sëmundjeve të ndryshme pulmonare dhe kronike.
3. Monoksidi i karbonit
 Një gaz pa ngjyrë, pa erë.
Një gaz pa ngjyrë, pa erë.
Përqendrimi i monoksidit të karbonit II në ajrin urban është më i madh se ai i çdo ndotësi tjetër. Megjithatë, duke qenë se ky gaz është pa ngjyrë, pa erë dhe pa shije, shqisat tona nuk janë në gjendje ta zbulojnë atë. Burimi më i madh i monoksidit të karbonit në qytete janë automjetet. Në shumicën e qyteteve, mbi 90% e monoksidit të karbonit hyn në ajër për shkak të djegies jo të plotë të karbonit në karburantin motorik sipas reaksionit: 2C + O2 = 2CO. Djegia e plotë prodhon dioksid karboni si produkt përfundimtar: C + O2 = CO2. Një tjetër burim i monoksidit të karbonit është tymi i duhanit, i cili haset jo vetëm nga njerëzit që pinë duhan, por edhe nga mjedisi i tyre i afërt. Është vërtetuar se një duhanpirës thith dy herë më shumë monoksid karboni sesa një jo duhanpirës. Monoksidi i karbonit thithet së bashku me ajrin ose tymin e duhanit dhe hyn në gjak, ku konkurron me oksigjenin për molekulat e hemoglobinës. Monoksidi i karbonit lidhet me molekulat e hemoglobinës më fort se sa oksigjeni. Sa më shumë monoksid karboni të ketë në ajër, aq më shumë hemoglobinë lidhet me të dhe aq më pak oksigjen arrin në qeliza. Aftësia e gjakut për të dhënë oksigjen në inde është e dëmtuar, shkaktohen spazma vaskulare dhe aktiviteti imunologjik i një personi zvogëlohet. Për këtë arsye, monoksidi i karbonit në përqendrime të larta është një helm vdekjeprurës. Monoksidi i karbonit hyn në atmosferë edhe nga ndërmarrjet industriale si rezultat i djegies jo të plotë të karburantit. Shumë monoksid karboni përmbahet në emetimet nga ndërmarrjet metalurgjike dhe petrokimike. I thithur në sasi të mëdha, monoksidi i karbonit hyn në gjak, rrit sasinë e sheqerit në gjak dhe dobëson furnizimin me oksigjen në zemër. Tek njerëzit e shëndetshëm, ky efekt manifestohet në një ulje të aftësisë për të toleruar ushtrime fizike. Tek njerëzit me sëmundje kronike të zemrës, mund të ndikojë në të gjithë funksionimin e trupit. Kur qëndrojnë në një autostradë të ngarkuar për 1-2 orë, disa njerëz me sëmundje të zemrës mund të përjetojnë simptoma të ndryshme të përkeqësimit të shëndetit.
4. Dioksidi i squfurit
Gaz pa ngjyrë me erë të fortë.
Në përqendrime të ulëta (20-30 mg/m3), dioksidi i squfurit krijon një shije të pakëndshme në gojë dhe irriton mukozën e syve dhe traktin respirator. Ai lëshohet në atmosferë kryesisht si rezultat i funksionimit të termocentraleve (TEC) gjatë djegies së qymyrit të murrmë dhe vajit të karburantit, si dhe produkteve të naftës që përmbajnë squfur dhe gjatë prodhimit të shumë metaleve nga xehet që përmbajnë squfur. - PbS, ZnS, CuS, NiS, MnS, etj. Kur digjet qymyri ose nafta, squfuri që ai përmban oksidohet, duke prodhuar dy përbërës - dioksid squfuri dhe trioksid squfuri. Kur tretet në ujë, dioksidi i squfurit formon shiun acid, i cili shkatërron bimët, acidifikon tokën dhe rrit aciditetin e liqeneve. Edhe me një përmbajtje mesatare të oksideve të squfurit në ajër prej rreth 100 μg/m3, që ndodh shpesh në qytete, bimët marrin një nuancë të verdhë. Pyjet halore dhe gjetherënëse janë më të ndjeshme ndaj tij. Me një përmbajtje të lartë të SO2 në ajër, pishat thahen. Është vërejtur se sëmundjet e rrugëve të frymëmarrjes, si bronkiti, bëhen më të shpeshta kur rritet niveli i oksideve të squfurit në ajër. Ekspozimi ndaj dioksidit të squfurit në përqendrime mbi MPC mund të shkaktojë mosfunksionim të frymëmarrjes dhe një rritje të konsiderueshme të sëmundjeve të ndryshme të frymëmarrjes; ka një efekt në mukozën, inflamacion të nazofaringit, trake, bronkit, kollë, ngjirurit e zërit dhe dhimbje të fytit. Veçanërisht ndjeshmëri e lartë ndaj efekteve të dioksidit të squfurit vërehet te njerëzit me çrregullime kronike të frymëmarrjes dhe astmë. Kur përqendrimet e kombinuara të dioksidit të squfurit dhe grimcave të pezulluara (në formën e blozës) mesatarisht në ditë janë mbi 200 μg/m3, vërehen ndryshime të lehta në aktivitetin e mushkërive tek të rriturit dhe fëmijët.
5. Benz(a)piren
Benz(a)pireni (BP) hyn në atmosferë gjatë djegies lloje të ndryshme karburant. Shumë BP janë të përfshira në emetimet nga metalurgjia me ngjyra dhe me ngjyra, energjia dhe Industria e ndërtimit. OBSH ka vendosur një vlerë mesatare vjetore prej 0,001 μg/m3 si vlerë mbi të cilën mund të vërehen efekte negative në shëndetin e njeriut, duke përfshirë shfaqjen e tumoreve malinje.
6. Plumbi
 Ndotja e ajrit nga plumbi krijohet nga ndërmarrjet e metalurgjisë, përpunimit të metaleve, inxhinierisë elektrike, petrokimike dhe transportit motorik. Pranë autostradave, përqendrimet e plumbit janë 2-4 herë më të larta se larg tyre. Plumbi prek njerëzit në shumë mënyra, duke përfshirë thithjen e ajrit që përmban plumb përmes ushqimit, ujit dhe pluhurit. 50% e këtij metali hyn në trup përmes sistemit të frymëmarrjes. Akumulohet në trup, kocka dhe inde sipërfaqësore. Plumbi ndikon në veshkat, mëlçinë, sistemin nervor dhe organet që prodhojnë gjak. Ka një efekt mutagjenik. Përbërjet organike të plumbit prishin metabolizmin. Komponimet e plumbit janë veçanërisht të rrezikshme për trupin e fëmijëve, pasi ato shkaktojnë sëmundje kronike të trurit që çojnë në prapambetje mendore. Rritja e trafikut të automjeteve dhe përdorimi i benzinës me plumb shoqërohet me rritje të emetimeve të plumbit nga automjetet.
Ndotja e ajrit nga plumbi krijohet nga ndërmarrjet e metalurgjisë, përpunimit të metaleve, inxhinierisë elektrike, petrokimike dhe transportit motorik. Pranë autostradave, përqendrimet e plumbit janë 2-4 herë më të larta se larg tyre. Plumbi prek njerëzit në shumë mënyra, duke përfshirë thithjen e ajrit që përmban plumb përmes ushqimit, ujit dhe pluhurit. 50% e këtij metali hyn në trup përmes sistemit të frymëmarrjes. Akumulohet në trup, kocka dhe inde sipërfaqësore. Plumbi ndikon në veshkat, mëlçinë, sistemin nervor dhe organet që prodhojnë gjak. Ka një efekt mutagjenik. Përbërjet organike të plumbit prishin metabolizmin. Komponimet e plumbit janë veçanërisht të rrezikshme për trupin e fëmijëve, pasi ato shkaktojnë sëmundje kronike të trurit që çojnë në prapambetje mendore. Rritja e trafikut të automjeteve dhe përdorimi i benzinës me plumb shoqërohet me rritje të emetimeve të plumbit nga automjetet.
7. Formaldehid
Gaz pa ngjyrë me erë të fortë irrituese.
Është pjesë e shumë materialeve artificiale: kompensatë, llaqe, kozmetikë, dezinfektues dhe substanca që përdoren në amvisëri. Formaldehidi gjendet në emetimet e dëmshme nga termocentralet dhe furrat e tjera industriale. Një sasi e caktuar formaldehidi formohet edhe kur pini cigare. Dhe së fundi, ajo gjendet kudo në natyrë, madje edhe në trupin e njeriut. Përqendrimet natyrore nuk ndikojnë në shëndetin e njeriut në asnjë mënyrë, por përqendrimet e larta të formaldehidit me origjinë artificiale janë të rrezikshme për të. Ato shkaktojnë dhimbje koke, humbje të vëmendjes dhe dhimbje në sy. Trakti i frymëmarrjes dhe mushkëritë, indet mukoze të traktit gastrointestinal janë të dëmtuara. Reaksionet alergjike të shkaktuara nga formaldehidi prishin funksionimin e organeve të brendshme dhe shkaktojnë sëmundje kronike. Gjithashtu preket aparati gjenetik, i cili mund të shkaktojë shfaqjen e tumoreve kancerogjene. Formaldehidi i lirë çaktivizon një sërë enzimash në organe dhe inde, pengon sintezën e acideve nukleike dhe prish metabolizmin e vitaminës C. Kur disa materiale digjen, formaldehidi formohet. Gjendet, për shembull, në tymrat e shkarkimit të makinave dhe tymin e cigareve. MAC-et e brendshme mund të tejkalohen lehtësisht vetëm për shkak të pirjes së duhanit.
8. Fenoli
 Substanca kristalore pa ngjyrë, më rrallë lëngje me valë të lartë me erë karakteristike të fortë.
Substanca kristalore pa ngjyrë, më rrallë lëngje me valë të lartë me erë karakteristike të fortë.
Monatomike - helme të forta nervore që shkaktojnë helmim të përgjithshëm të trupit edhe përmes lëkurës, i cili ka një efekt kauterizues. Poliatomike - mund të shkaktojë sëmundje të lëkurës; me marrje të zgjatur në trup, ato mund të pengojnë enzimat. Produktet e oksidimit të fenoleve janë më pak toksike. Fenoli teknik është një lëng viskoz i kuq-kafe, ndonjëherë i zi. Fenoli përdoret kryesisht për sintezën e fenol-formaldehidit dhe rrëshirave të tjera dhe një sërë përbërjesh aromatike; për dezinfektim. Fenoli dhe derivatet e tij janë ndër komponimet toksike më të rrezikshme që gjenden në ujërat e zeza nga një sërë industrish. Shenjat e helmimit fenolik janë një gjendje eksitimi dhe një rritje e aktivitetit motorik, duke u kthyer në konvulsione, të cilat tregojnë mosfunksionim. sistemi nervor, dhe, para së gjithash, sistemi neuromuskular. Në rast helmimi kronik vërehet acarim i rrugëve të frymëmarrjes, dispepsi, nauze, të vjella në mëngjes, dobësi e përgjithshme dhe muskulare, kruajtje, nervozizëm dhe pagjumësi.
9. Klori
Gaz me erë të pakëndshme dhe specifike.
Burimet kryesore të ekspozimit të klorit që lidhen me shëndetin e njeriut janë emetimet industriale. Klori është gërryes ndaj shumicës së materialeve të ndërtimit, si dhe pëlhurave. Sistemet teknologjike që përmbajnë klor mbahen të mbyllura. Ekspozimi vërehet kryesisht si rezultat i performancës së dobët të bimëve ose lëshimeve aksidentale. Kur lëshohet, përhapet poshtë në tokë. Në përqendrime të ulëta, efektet akute të ekspozimit ndaj klorit zakonisht kufizohen në një erë të fortë dhe acarim të lehtë të syve dhe traktit të sipërm respirator. Këto dukuri zhduken menjëherë pas ndërprerjes së ekspozimit. Me rritjen e përqendrimeve, simptomat bëhen më të theksuara dhe trakti i poshtëm i frymëmarrjes përfshihet në proces. Përveç acarimit të menjëhershëm dhe kollës së shoqëruar, viktimat përjetojnë ankth. Ekspozimi ndaj klorit në përqendrime më të larta karakterizohet nga gulçim, cianozë, të vjella, dhimbje koke dhe agjitacion të shtuar, veçanërisht në individë të prirur ndaj reaksioneve neurotike. Vëllimi i baticës zvogëlohet dhe mund të zhvillohet edema pulmonare. Me trajtim, shërimi zakonisht ndodh brenda 2-14 ditëve. Në rastet më të rënda, duhet të priten komplikime të tilla si pneumonia infektive ose aspirative.
10. Arseniku
Arseniku dhe komponimet e tij. - Arsenati i kalciumit, arseniti i natriumit, jeshilja pariziane dhe komponime të tjera që përmbajnë arsenik përdoren si pesticide për trajtimin e farave dhe kontrollin e dëmtuesve bujqësorë; ato janë fiziologjikisht aktive dhe helmuese. Doza vdekjeprurëse kur merret nga goja është 0,06-0,2 g. Përbërjet e tij të tretshme (anhidridet, arsenatet dhe arsenitet), kur hyjnë me ujë në traktin gastrointestinal, absorbohen lehtësisht nga mukoza, hyjnë në qarkullimin e gjakut dhe barten nga ajo në të gjithë. organet ku dhe grumbullohen. Simptomat e helmimit me arsenik janë një shije metalike në gojë, të vjella, dhimbje të forta barku. Më vonë, konvulsione, paralizë, vdekje. Antidoti më i njohur dhe më i disponueshëm për helmimin me arsenik është qumështi, ose më mirë proteina kryesore e qumështit, kazeina, e cila formon një përbërës të patretshëm me arsenikun që nuk përthithet në gjak. Helmimi kronik me arsenik çon në humbje të oreksit dhe sëmundje gastrointestinale.
11. Kancerogjenet
Substancat që kanë aftësinë të shkaktojnë zhvillimin e tumoreve malinje.
Ndër substancat që hyjnë në mjedisin e ajrit dhe ujit, kancerogjenët janë zinku, arseniku, plumbi, kromi, nitratet, jodi, benzili, DDT dhe mangani. Molibden, plumbi dhe bakri shkaktojnë çrregullime të sistemit nervor qendror; brom, barium dhe kadmium - dëmtim i veshkave; merkuri dhe hekuri janë sëmundje të gjakut.
12. Ozoni (niveli i tokës)
Një substancë e gaztë (në kushte normale), molekula e së cilës përbëhet nga tre atome oksigjeni. Në kontakt të drejtpërdrejtë vepron si një agjent i fortë oksidues.
Shkatërrimi i shtresës së ozonit çon në një rritje të fluksit të rrezatimit UV në sipërfaqen e tokës, gjë që çon në një rritje të rasteve të kancerit të lëkurës, kataraktave dhe dobësimit të imunitetit. Ekspozimi i tepërt ndaj ultravjollcës çon në një rritje të incidencës së melanomës, llojit më të rrezikshëm të kancerit të lëkurës.
Ozoni i nivelit të tokës nuk lëshohet drejtpërdrejt në ajër, por prodhohet nga reaksionet kimike midis oksideve të azotit (NOx) dhe përbërjeve organike të avullueshme (VOCs) në prani të rrezatimit diellor. Emetimet nga ndërmarrjet industriale dhe termocentralet, shkarkimet e automjeteve, avujt e benzinës dhe tretësit kimikë janë burimet kryesore të NOx dhe VOC.
Në nivelin e sipërfaqes së tokës, ozoni është një ndotës i dëmshëm. Ndotja e ozonit përbën një kërcënim gjatë muajve të verës pasi rrezatimi intensiv diellor dhe moti i nxehtë kontribuojnë në formimin e përqendrimeve të dëmshme të ozonit në ajrin që thithim. Thithja e ozonit mund të shkaktojë një sërë problemesh shëndetësore, duke përfshirë dhimbje gjoksi, kollë, acarim të fytit dhe skuqje të trupit. Mund të përkeqësojë gjendjen e pacientëve me bronkit, emfizemë dhe astmë. Ozoni i nivelit të tokës mund të dëmtojë funksionin e mushkërive dhe të çojë në inflamacion të mushkërive. Ekspozimi i përsëritur ndaj niveleve të larta të ozonit mund të shkaktojë dhëmbëza në mushkëri.
13. Amoniaku
Gaz i ndezshëm. Digjet në prani të një burimi të vazhdueshëm zjarri. Avujt formojnë përzierje shpërthyese me ajrin. Kontejnerët mund të shpërthejnë kur nxehen. Përzierjet shpërthyese formohen në enë boshe.
E dëmshme nëse thithet. Avujt janë shumë irritues për mukozën dhe lëkurën dhe shkaktojnë ngrirje. Adsorbohet nga veshjet.
Në rast helmimi, dhimbje djegëse në fyt, kollë e fortë, ndjenjë mbytjeje, djegie të syve dhe lëkurës, agjitacion të fortë, marramendje, të përzier, dhimbje stomaku, të vjella, spazma e glotisit, mbytje, deliri i mundshëm, humbja e vetëdije, konvulsione dhe vdekje (për shkak të dobësisë kardiake ose ndalimit të frymëmarrjes). Vdekja më së shpeshti ndodh brenda pak orësh ose ditësh si pasojë e ënjtjes së laringut ose mushkërive.
14. Sulfidi i hidrogjenit
Gaz pa ngjyrë me erë të pakëndshme. Më e rëndë se ajri. Le të tretemi në ujë. Grumbullohet në zona të ulëta të sipërfaqes, bodrume, tunele.
Gaz i ndezshëm. Avujt formojnë përzierje shpërthyese me ajrin. Ndizet lehtë dhe digjet me një flakë blu të zbehtë.
Simptomat e helmimit: dhimbje koke, acarim në hundë, shije metalike në gojë, nauze, të vjella, djersë të ftohtë, rrahje të rrahura, shtrydhje të kokës, të fikët, dhimbje gjoksi, mbytje, djegie sysh, lakrimim, fotofobi, mund të jenë fatale nëse thithen. .
15. Fluori i hidrogjenit
Lëng ose gaz pa ngjyrë, me valë të ulët, me erë të fortë. Më e rëndë se ajri. Le të tretemi në ujë. Pi duhan në ajër. Korrozive. Grumbullohet në pjesë të ulëta të sipërfaqes, bodrume, tunele.
Jo i ndezshëm. Lëshon gaz të ndezshëm në kontakt me metalet. Helmues nëse merret nga goja. Mundësisht fatale nëse thithet. Vepron përmes lëkurës së dëmtuar. Avujt janë shumë irritues për mukozën dhe lëkurën. Kontakti me lëngun shkakton djegie të lëkurës dhe syve.
Simptomat e helmimit: acarim dhe tharje të mukozës së hundës, teshtitje, kollë, mbytje, nauze, të vjella, humbje të vetëdijes, skuqje dhe kruajtje të lëkurës.
16. Klorur hidrogjeni
Gaz pa ngjyrë me erë të fortë. Në ajër, duke ndërvepruar me avujt e ujit, formon një mjegull të bardhë të acidit klorhidrik. Jashtëzakonisht i tretshëm në ujë.
Kloruri i hidrogjenit ka veti të forta acidike. Reagon me shumicën e metaleve për të formuar kripëra dhe për të lëshuar gaz hidrogjen.
Për shkak të tretshmërisë jashtëzakonisht të lartë në ujë, helmimi zakonisht nuk ndodh me gaz klorur hidrogjeni, por me një mjegull acidi klorhidrik. Zona kryesore e prekur është trakti i sipërm respirator, ku pjesa më e madhe e acidit neutralizohet. Është e nevojshme të merret parasysh kontaminimi i emetimeve me substanca të tjera, si dhe mundësia e formimit të reagentëve toksikë, veçanërisht arsinës (AsH3).
17. Acidi sulfurik
Lëng vajor, pa ngjyrë dhe pa erë. Një nga acidet më të forta. Prodhuar nga djegia e squfurit ose mineraleve të pasura me squfur; dioksidi i squfurit që rezulton oksidohet në gaz squfuri anhidrik, i cili absorbohet nga uji për të formuar acid sulfurik.
Acidi sulfurik është një nga produktet kryesore industria kimike. Përdoret për prodhimin e plehrave minerale (superfosfat, sulfat amoniumi), acide dhe kripëra të ndryshme, ilaçe dhe detergjentë, ngjyra, fibra artificiale dhe eksplozivë.
Përdoret në metalurgji (zbërthimi i xeheve, si uraniumi), për pastrimin e produkteve të naftës, si tharës, etj.
Ajo ka një efekt shkatërrues në indet dhe substancat bimore dhe shtazore, duke u hequr ujin, si rezultat i së cilës ato shkrumbohen.
18. Bakri
Bakri është një metal i verdhë-portokalli me një nuancë të kuqe dhe ka përçueshmëri të lartë termike dhe elektrike.
Bakri hyn në mjedis nga pllakat e bakrit, tunxhimi, banjot e bronzimit, nga banjot për heqjen e veshjes së bakrit dhe nga banjot e gravurës së bakrit të mbështjellë dhe tombakut, si dhe gjatë gravurjes së pllakave të qarkut të printuar.
Bakri ndikon në sistemin e frymëmarrjes, metabolizmin, alergjen. Me praninë e njëkohshme të metaleve të rënda, janë të mundshme tre lloje të vetive toksike:
1. Sinergizmi - efekti i veprimit është më i madh se efekti total (kadmiumi në kombinim me zink dhe cianide);
2. Antagonizmi - efekti i një veprimi është më i vogël se efekti i përgjithshëm. Për shembull, me praninë e kombinuar të bakrit dhe zinkut, toksiciteti i përzierjes zvogëlohet me 60-70%;
3. Aditiv - efekt veprimi e barabartë me shumën efektet toksike të çdo metali të rëndë (përzierje sulfidesh zinku dhe bakri në përqendrime të ulëta).
Avujt e metaleve të bakrit të krijuara gjatë prodhimit të lidhjeve të ndryshme mund të hyjnë në trup me ajër të thithur dhe të shkaktojnë helmim.
Thithja e përbërjeve të bakrit nga stomaku në gjak ndodh ngadalë. Meqenëse kripërat e bakrit që hyjnë në stomak shkaktojnë të vjella, ato mund të ekskretohen nga stomaku me të vjella. Prandaj, vetëm sasi të vogla të bakrit hyjnë në gjak nga stomaku. Kur komponimet e bakrit hyjnë në stomak, funksionet e tij mund të ndërpriten dhe mund të shfaqet diarre. Pasi komponimet e bakrit absorbohen në gjak, ato veprojnë në kapilarët, duke shkaktuar hemolizë, dëmtim të mëlçisë dhe veshkave. Kur solucionet e koncentruara të kripërave të bakrit futen në sy në formën e pikave, mund të zhvillohet konjuktiviti dhe mund të ndodhë dëmtimi i kornesë.
19. Kadmium
Kadmiumi është një metal i bardhë argjendi, blu vezullues, i butë dhe i shkrirë, i cili zbehet në ajër për shkak të formimit të një filmi oksidi mbrojtës.
Vetë metali nuk është toksik, por komponimet e tretshme të kadmiumit janë jashtëzakonisht toksike. Për më tepër, çdo mënyrë e hyrjes së tyre në trup dhe në çdo gjendje (tretësirë, pluhur, tym, mjegull) është e rrezikshme. Për sa i përket toksicitetit, kadmiumi nuk është inferior ndaj merkurit dhe arsenikut. Përbërjet e kadmiumit kanë një efekt depresiv në sistemin nervor, ndikojnë në traktin respirator dhe shkaktojnë ndryshime në organet e brendshme.
Përqendrimet e mëdha të kadmiumit mund të çojnë në helmim akut: një minutë qëndrim në një dhomë që përmban 2500 mg/m 3 përbërës të tij çon në vdekje. Në helmimin akut, simptomat e dëmtimit nuk zhvillohen menjëherë, por pas një periudhe të caktuar latente, e cila mund të zgjasë nga 1-2 deri në 30-40 orë.
Pavarësisht toksicitetit të tij, kadmiumi është vërtetuar të jetë një element gjurmë jetik për zhvillimin e organizmave të gjallë.
20. Berilium
Beriliumi është metali i dytë më i lehtë i njohur. Për shkak të vetive të tyre, beriliumi dhe lidhjet e tij përdoren gjerësisht në industri. Disa lëndë djegëse, si qymyri dhe nafta, përmbajnë pjesë të beriliumit, kështu që ky element gjendet në ajër dhe në indet e gjalla të banorëve të qytetit. Djegia e mbeturinave dhe mbeturinave është gjithashtu një burim i ndotjes së ajrit. Në thelb, beriliumi mund të gëlltitet përmes thithjes së pluhurit ose tymrave, si dhe përmes kontaktit me lëkurën.
Toksiciteti i beriliumit është i njohur që nga vitet '30 të shekullit të njëzetë, dhe që nga vitet '50 është njohur si i rrezikshëm për njerëzit dhe mjedisin. Falë masave të sigurisë të marra, format akute të beriliozës janë zhdukur praktikisht, por rastet kronike vazhdojnë të regjistrohen. Një tipar dallues i sëmundjeve kronike të shkaktuara nga beriliumi (CBD) është aftësia e tyre për t'u maskuar si sarkoidozë (sëmundja e Beck), kështu që CBD është shumë e vështirë për t'u identifikuar.
Sarkoidoza shkakton granuloma në mushkëri, mëlçi, shpretkë dhe zemër. Sëmundja e lëkurës zhvillohet dhe vërehet një dobësim i fortë i sistemit imunitar. NË formë kronike berilioza karakterizohet nga gulçim i rëndë, kollë, lodhje, dhimbje gjoksi, humbje peshe, djersitje e shtuar, ethe dhe ulje e oreksit. Koha e kaluar nga kontakti i parë me beriliumin deri në shfaqjen e shenjave klinike mund të ndryshojë nga disa muaj në disa dekada. Në një fazë të hershme, sëmundja shoqërohet me një shkelje të shkëmbimit të ajrit në mushkëri, dhe në një fazë të vonë ka një ndërprerje pothuajse të plotë të shkëmbimit të ajrit.
Po kështu, pneumoniti akut, pneumoniti kronik, sarkoidoza dhe berilioza akute - të gjitha këto janë format më të rrezikshme të sëmundjeve kronike.
21. Mërkuri
Mërkuri është një metal i rëndë argjend-bardhë, i vetmi metal që është i lëngshëm në kushte normale.
Helmimi nga mërkuri dhe komponimet e tij është i mundur në miniera dhe fabrika të merkurit, gjatë prodhimit të instrumenteve të caktuara matëse, llambave, farmaceutikëve, insektofungicideve etj.
Rreziku kryesor është avulli i merkurit metalik, lëshimi i të cilit nga sipërfaqet e hapura rritet me rritjen e temperaturës së ajrit. Kur thithet, merkuri hyn në qarkullimin e gjakut. Në trup, merkuri qarkullon në gjak, duke u kombinuar me proteinat; depozitohet pjesërisht në mëlçi, veshka, shpretkë, indet e trurit etj. Efekti toksik shoqërohet me bllokimin e grupeve sulfhidrile të proteinave të indeve, ndërprerjen e aktivitetit të trurit (kryesisht hipotalamusin). Mërkuri ekskretohet nga trupi nëpërmjet veshkave, zorrëve, gjëndrave të djersës etj.
Helmimi akut me merkur dhe avujt e tij është i rrallë. Në helmimet kronike, vërehet paqëndrueshmëri emocionale, nervozizëm, ulje e performancës, shqetësim i gjumit, dridhje gishtash, ulje e nuhatjes dhe dhimbje koke. Një shenjë karakteristike e helmimit është shfaqja e një kufiri blu-zi përgjatë skajit të mishrave të dhëmbëve; Dëmtimi i mishrave të dhëmbëve (lirshmëria, gjakderdhja) mund të çojë në gingivit dhe stomatit. Në rast helmimi me komponime organike të merkurit (fosfat dietilmerkur, dietilmerkur, klorur etilmerkurik), mbizotërojnë shenjat e dëmtimit të njëkohshëm të sistemit nervor qendror (encefalo-polineuriti) dhe kardiovaskular, stomakut, mëlçisë dhe veshkave.
22. Zinku
Zinku është një metal i bardhë-kaltërosh. Ai luan një rol të rëndësishëm në sintezën e acideve nukleike dhe proteinave. Elementi është i nevojshëm për stabilizimin e strukturës së ADN-së, ARN-së, ribozomeve, luan një rol të rëndësishëm në procesin e përkthimit dhe është i domosdoshëm në shumë faza kyçe të shprehjes së gjeneve.
Përqendrimet e ngritura të zinkut kanë një efekt toksik në organizmat e gjallë. Tek njerëzit, ato shkaktojnë nauze, të vjella, dështim të frymëmarrjes, fibrozë pulmonare dhe janë kancerogjene. Zinku i tepërt në bimë ndodh në zonat e ndotjes industriale të tokës, si dhe me përdorimin e pahijshëm të plehrave që përmbajnë zink.
Monoksidi i karbonit (monoksidi i karbonit).
Oksid karboni- gaz pa ngjyrë, pa erë, pak më i lehtë se ajri, pak i tretshëm në ujë, ka një pikë vlimi: - 191,5°C. Në ajër ndizet në një temperaturë prej 700°C dhe digjet me një flakë blu në CO 2 .
Burimet e hyrjes në mjedis.
Monoksidi i karbonit është pjesë e atmosferës (10%). Monoksidi i karbonit hyn në atmosferë si pjesë e gazeve vullkanike dhe kënetore, si rezultat i zjarreve të pyjeve dhe stepave dhe emetimit nga mikroorganizmat, bimët, kafshët dhe njerëzit. Nga shtresat sipërfaqësore të oqeaneve, 220 x 10 6 ton monoksid karboni çlirohen në vit si rezultat i fotodekompozimit të algave të kuqe, blu-jeshile dhe të tjera, produkte të mbeturinave të planktonit. Niveli natyror i monoksidit të karbonit në ajrin atmosferik është 0,01-0,9 mg/m3.
Monoksidi i karbonit hyn në atmosferë nga ndërmarrjet industriale, kryesisht nga metalurgjia. Në proceset metalurgjike, kur shkrihen 1 milion ton çeliku, formohen 320-400 ton monoksid karboni. Një sasi e madhe CO formohet në industrinë e naftës dhe në impiantet kimike (plasaritje e naftës, prodhimi i formaldehidit, hidrokarbureve, amoniakut, etj.). Një burim tjetër i rëndësishëm i monoksidit të karbonit është tymi i duhanit. Përqendrimi i monoksidit të karbonit është i lartë në minierat e qymyrit dhe në rrugët e furnizimit me qymyr. Monoksidi i karbonit formohet gjatë djegies jo të plotë të karburantit në soba dhe motorë me djegie të brendshme. Një burim i rëndësishëm i monoksidit të karbonit është transporti rrugor.
Si rezultat i aktivitetit njerëzor, çdo vit në atmosferë hyjnë 350-600x10 6 ton monoksid karboni. Rreth 56-62% e kësaj sasie vjen nga automjetet (përmbajtja e monoksidit të karbonit në gazrat e shkarkimit mund të arrijë në 12%).
Sjellja në mjedisi.
Në kushte normale, monoksidi i karbonit është inert. Nuk ndërvepron kimikisht me ujin. Tretshmëria e CO në ujë është rreth 1:40 për nga vëllimi. Në tretësirë është në gjendje të reduktojë kripërat e arit dhe platinit në metale të lira tashmë në temperaturë normale. CO gjithashtu nuk reagon me alkalet dhe acidet. Ndërvepron me alkalet kaustike vetëm në temperatura të ngritura dhe presione të larta.
Humbja e monoksidit të karbonit në mjedis ndodh për shkak të dekompozimit të tij nga kërpudhat e tokës. Përveç kësaj, kur ka një tepricë të oksigjenit në tokat me përbërje të rëndë mekanike, të pasura me lëndë organike, ndodh kalimi i CO në CO 2.
Ndikimi në trupin e njeriut.
Monoksidi i karbonit është jashtëzakonisht helmues. Përmbajtja e lejuar e CO në ambientet industriale është 20 mg/m 3 gjatë ditës së punës, 50 mg/m 3 për 1 orë, 100 mg/m 3 për 30 minuta, në ajrin atmosferik të qytetit maksimumi një herë (në 20 minuta) është 5 mg/m3, MPC mesatare ditore - 3 mg/m3. Niveli natyror i monoksidit të karbonit në ajrin atmosferik është 0,01-0,9 mg/m3.
CO thithet së bashku me ajrin dhe hyn në gjak, ku konkurron me oksigjenin për molekulat e hemoglobinës. Monoksidi i karbonit, që ka një lidhje kimike të dyfishtë, lidhet me hemoglobinën më fort se një molekulë oksigjeni. Sa më shumë CO2 të jetë në ajër, aq më shumë molekula të hemoglobinës lidhen me të dhe aq më pak oksigjen arrin në qelizat e trupit. Aftësia e gjakut për të dhënë oksigjen në inde është ndërprerë, shkaktohen spazma vaskulare, ulet aktiviteti imunologjik i një personi, i shoqëruar me dhimbje koke, humbje të vetëdijes dhe vdekje. Për këto arsye, CO në përqëndrime të larta është një helm vdekjeprurës.
CO prish metabolizmin e fosforit. Shkelja e metabolizmit të azotit shkakton sotemi, ndryshime në përmbajtjen e proteinave plazmatike, ulje të aktivitetit të kolinesterazës në gjak dhe nivelit të vitaminës B 6. Monoksidi i karbonit ndikon në metabolizmin e karbohidrateve, rrit zbërthimin e glikogjenit në mëlçi, duke ndërprerë përdorimin e glukozës, duke rritur nivelin e sheqerit në gjak. Hyrja e CO nga mushkëritë në gjak përcaktohet nga përqendrimi i CO në ajrin e thithur dhe kohëzgjatja e thithjes. CO çlirohet kryesisht përmes rrugëve të frymëmarrjes.
Sistemi nervor qendror vuan më së shumti nga helmimi. Kur thithni një përqendrim të vogël (deri në 1 mg/l) - rëndim dhe ndjenjë e shtrydhjes së kokës, dhimbje të forta në ballë dhe në tëmth, marramendje, dridhje, etje, rritje të rrahjeve të zemrës, nauze, të vjella, rritje të temperaturës së trupit në 38-40 ° C. Dobësia në këmbë tregon se veprimi është përhapur në palcën kurrizore.
Toksiciteti ekstrem i CO, mungesa e ngjyrës dhe erës së tij, si dhe përthithja shumë e dobët e tij nga karboni i aktivizuar i një maskë gazi konvencionale e bëjnë këtë gaz veçanërisht të rrezikshëm.
Amoniaku.

Amoniaku- gaz pa ngjyrë me erë të fortë, pikë shkrirjeje - 80°C, pikë vlimi - 36°C, i tretshëm në ujë, alkool dhe një sërë tretësish të tjerë organikë. Sintetizohet nga azoti dhe hidrogjeni. Në natyrë, ajo formohet gjatë dekompozimit të azotit që përmban komponimet organike.
Të qenit në natyrë.
Në natyrë, ajo formohet gjatë dekompozimit të përbërjeve organike që përmbajnë azot.
Era e mprehtë e amoniakut është e njohur për njeriun që në kohët parahistorike, pasi ky gaz formohet në sasi të konsiderueshme gjatë kalbjes, dekompozimit dhe distilimit të thatë të përbërjeve organike që përmbajnë azot, si ure ose proteina. Është e mundur që në fazat e hershme të evolucionit të Tokës të ketë pasur mjaft amoniak në atmosferën e saj. Megjithatë, edhe tani, sasi të vogla të këtij gazi mund të gjenden gjithmonë në ajër dhe në ujërat e shiut, pasi ai formohet vazhdimisht gjatë dekompozimit të proteinave shtazore dhe bimore.
Burimet antropogjene të hyrjes në mjedis.
Burimet kryesore të emetimeve të amoniakut janë impiantet e plehrave azotike, ndërmarrjet për prodhimin e acidit nitrik dhe kripërave të amonit, njësitë ftohëse, fabrikat e koksit dhe fermat blegtorale. Në zonat me ndotje teknogjene, përqendrimet e amoniakut arrijnë vlerat 0,015-0,057 mg/m3, në zonat e kontrollit - 0,003-0,005 mg/m3.
Efekti në trupin e njeriut.
Ky gaz është toksik. Një person është në gjendje të nuhasë amoniakun në ajër tashmë në një përqendrim të parëndësishëm - 0.0005 mg / l, kur ende nuk ka ndonjë rrezik të madh për shëndetin. Kur përqendrimi rritet 100 herë (deri në 0,05 mg/l), manifestohet efekti irritues i amoniakut në mukozën e syve dhe në traktin e sipërm respirator, madje është i mundur edhe një ndërprerje refleksive e frymëmarrjes. Edhe një person shumë i shëndetshëm vështirë se mund të përballojë një përqendrim prej 0,25 mg/l për një orë. Edhe përqendrimet më të larta shkaktojnë djegie kimike të syve dhe rrugëve të frymëmarrjes dhe bëhen të rrezikshme për jetën. Shenjat e jashtme të helmimit me amoniak mund të jenë mjaft të pazakonta. Tek viktimat, për shembull, pragu i dëgjimit zvogëlohet ndjeshëm: edhe tingujt jo shumë të lartë bëhen të padurueshëm dhe mund të shkaktojnë konvulsione. Helmimi me amoniak gjithashtu shkakton agjitacion të fortë, madje edhe deliri të dhunshëm, dhe pasojat mund të jenë shumë të rënda - duke çuar në një ulje të inteligjencës dhe ndryshimeve të personalitetit. Natyrisht, amoniaku mund të sulmojë qendrat vitale, kështu që duhet të merren masa paraprake të kujdesshme kur punoni me të.
Ekspozimi kronik ndaj dozave nënvdekjeprurëse të amoniakut çon në çrregullime autonome, rritje të ngacmueshmërisë së sistemit nervor parasimpatik, ankesa për dobësi, keqtrajtim, rrjedhje hundësh, kollë dhe dhimbje gjoksi.
Klasa e rrezikut të substancave - 4.
1 ujë përmban oksigjen
2 peshq thithin oksigjen të tretur në ujë
3 Ena është e mbushur me oksigjen
4 Plumbi grafit i lapsit përfaqëson karbonin
5 Ajri përmban azot
6 Azoti është një gaz pa ngjyrë, pak më i lehtë se ajri
hidrogjeni. Si rezultat, kemi marrë gaz pa ngjyrë B me një erë karakteristike të athët, i cili tretet mirë në ujë. tretësira B, e cila është e aftë të ngjyros fenolftaleinën e kuqe, substancën B të gaztë (n.s.) të përthithur, të përftuar nga veprimi i acidit sulfurik të koncentruar në kripën e tryezës. Në këtë rast, u formua një tretësirë e kripës G, kur i shtohej një tretësire e nitratit të argjendit (I), u precipitua një precipitat D i bardhë djathi.
Lëngu pa ngjyrë A u ngroh me zink dhe u lëshua gazi B, pa ngjyrë dhe praktikisht pa erë, pak më i lehtë se ajri. Kur oksidohet nga oksigjeni nënë prani të klorureve të paladiumit dhe bakrit, B shndërrohet në C. Kur avujt e substancës C kalojnë së bashku me hidrogjenin mbi një katalizator të ngrohur të nikelit, formohet komponimi D.
Zgjidhni këto substancat A-D:
1) CO
2) CH3-CH2-Br.
3) CH3-CH2-OH
4) CH2=CH2
5) CH2Br-CH2Br
6) CH3-CH=O
në oksigjen, nuk u zbulua ujë në produktet e reaksionit, por gjatë djegies së gazit B, uji zbulohet. Çfarë mase e një zgjidhjeje 15% të ujit gëlqeror do të kërkohet për të thithur produktet e djegies së gazeve A dhe B për të formuar një kripë acidi? 2.dioksidi i karbonit i formuar gjatë djegies së plotë të 0,1 mol të një alkani të panjohur u kalua përmes një tepricë uji gëlqeror. Në këtë rast kanë rënë 40 gram precipitat i bardhë. Përcaktoni formulën molekulare të këtij hidrokarburi 3. Një përzierje e karbonateve të bariumit dhe natriumit me peshë 150 gram u tretën në acid klorhidrik të tepërt. Një tepricë e tretësirës së sulfatit të natriumit iu shtua tretësirës që rezulton. Në këtë rast kanë rënë 34,95 gram sediment. përcaktoni fraksionet masive të karbonateve në përzierje. 4. jepen 10 gramë përzierje alumini, magnezi dhe oksidi i silikonit IV. Kur u tret në një tretësirë të koncentruar të hidroksidit të natriumit, u përftuan 6,72 litra hidrogjen. Kur e njëjta përzierje u tret në acid klorhidrik, u përftuan 8,96 litra hidrogjen. Llogaritni fraksionet masive të përbërësve të përzierjes. 5. Oksidi i fosforit i përftuar nga djegia e fosforit është tretur në një tretësirë 25% të hidroksidit të natriumit (p = 1,28 g/ml) për të formuar 24 gram dihidrogjen fosfat natriumi. Llogaritni masën e fosforit të oksiduar dhe vëllimin e alkalit të përdorur 6. Prodhuesi ftohje pajisje « Electrolux» V cilësisë ftohës përdor hidrokarbure, ciklike ndërtesat, duke pasur dendësia Nga metani 4 ,375 . Përcaktoni molekulare formulë kjo hidrokarbure

1. Gaz pa ngjyrë, pa erë. 2. Më i rëndë se ajri, 3. Helmues, 4. Shumë i tretshëm në ujë, 5. I tretshëm dobët në ujë, 6. Pak më i lehtë se ajri, 7. Shfaq veti acidike. 8. Oksid që nuk krijon kripë. 9. Kombinohet me hemoglobinën e gjakut, 10. Përftohet nga zbërthimi i karbonateve. 11. Në presion të lartë lëngëzohet, duke formuar “akull të thatë”, 12. Përdoret për prodhimin e sodës, 13. Përdoret si lëndë djegëse gazi, 14. Përdoret në prodhimin e ujërave frutash, 15. Përdoret në sintezën organike. 1. Gaz pa ngjyrë, pa erë. 2. Më i rëndë se ajri, 3. Helmues, 4. Shumë i tretshëm në ujë, 5. I tretshëm dobët në ujë, 6. Pak më i lehtë se ajri, 7. Shfaq veti acidike. 8. Oksid që nuk krijon kripë. 9. Kombinohet me hemoglobinën e gjakut, 10. Përftohet nga zbërthimi i karbonateve. 11. Në presion të lartë lëngëzohet, duke formuar “akull të thatë”, 12. Përdoret për prodhimin e sodës, 13. Përdoret si lëndë djegëse gazi, 14. Përdoret në prodhimin e ujërave frutash, 15. Përdoret në sintezën organike.

Acidi karbonik H 2 CO 3 Mr(H 2 CO 3) = =62 Acidi karbonik H 2 CO 3 Mr(H 2 CO 3) = =62



Meqenëse acidi karbonik është dybazik, ai formon dy lloje kripërash: karbonatet dhe bikarbonatet (Na 2 CO 3, NaHCO 3) Karbonatet e metaleve alkaline dhe amoniumi janë shumë të tretshëm në ujë, karbonatet e metaleve alkaline tokësore dhe disa të tjera janë praktikisht të patretshme në ujë. Karbonatet e aluminit, hekurit dhe kromit nuk mund të ekzistojnë në tretësirat ujore, pasi ato i nënshtrohen hidrolizës së plotë. Pothuajse të gjitha hidrokarbonatet janë të tretshme në ujë.Meqenëse acidi karbonik është dybazik, ai formon dy lloje kripërash: karbonatet dhe hidrokarbonatet (Na 2 CO 3, NaHCO 3) Karbonatet e metaleve alkaline dhe amoniumi janë shumë të tretshëm në ujë, karbonatet e tokës alkaline. metalet dhe disa të tjerë janë praktikisht të patretshëm në ujë. . Karbonatet e aluminit, hekurit dhe kromit nuk mund të ekzistojnë në tretësirat ujore, pasi ato i nënshtrohen hidrolizës së plotë. Pothuajse të gjitha bikarbonatet janë të tretshme në ujë


Na 2 CO 3 – Hiri i sodës – përdoret për prodhimin e alkaleve, në prodhimin e qelqit dhe në jetën e përditshme si detergjent. NaHCO 3 - sode buke ose sodë e pijshme - përdoret në industrinë ushqimore, për karikimin e aparateve të zjarrit dhe në mjekësi për urthin. (CuOH) 2 CO 3 – malakit – në piroteknikë, për prodhimin e bojrave minerale, në natyrë në formën e mineralit malakit (guri zbukurues) CaCO 3 – shkumës, gëlqeror, mermer – për prodhimin e gëlqeres, mermerit si gur mbarimi, në bujqësi për gëlqerimin e tokës K 2 CO 3 – potas – për prodhimin e sapunit, xhamit zjarrdurues, në fotografi. Na 2 CO 3 *10H 2 O - karbonat natriumi kristalor - konsumohet nga industria e sapunit, qelqit, tekstilit, letrës dhe naftës. Na 2 CO 3 – Hiri i sodës – përdoret për prodhimin e alkaleve, në prodhimin e qelqit dhe në jetën e përditshme si detergjent. NaHCO 3 - sode buke ose sodë e pijshme - përdoret në industrinë ushqimore, për karikimin e aparateve të zjarrit dhe në mjekësi për urthin. (CuOH) 2 CO 3 – malakit – në piroteknikë, për prodhimin e bojrave minerale, në natyrë në formën e mineralit malakit (guri zbukurues) CaCO 3 – shkumës, gëlqeror, mermer – për prodhimin e gëlqeres, mermerit si gur mbarimi, në bujqësi për gëlqerimin e tokës K 2 CO 3 – potas – për prodhimin e sapunit, xhamit zjarrdurues, në fotografi. Na 2 CO 3 *10H 2 O - karbonat natriumi kristalor - konsumohet nga industria e sapunit, qelqit, tekstilit, letrës dhe naftës.